簡介
歐盟醫療器材條例,MDR, 2017/745,附錄一:共通安全性與性能要求,第一章:一般要求,第6條(GSPR 6):「如器材在正常使用環境中使用,並根據製造商提供說明執行合宜維護,在製造商宣稱使用期的期間內,器材的特性和性能不應造成患者或使用者的健康或安全損害、(適用時)亦包括其他人員。」為符合GSPR第6條要求,製造商須決定係稱醫療器材的生命期(lifetime),評鑑該器材生命期的安全性與性能。
製造商規劃市場行銷策略、維修制度時,須慮及器材的生命期,乃至整個生命期的後市場監督計畫。又倘若生命期涉及器材的安全性與性能,則製造商務須告知使用者,當器材性能變化時,使用者應採取的措施,及如何處理器材的使用末期和結束使用階段的作業,按部就班地執行,包括所有警示標誌及防範措施,以便順利達成安全銷毀作業,參見該條例附錄一第二章第23條:標籤與使用說明書。
此文參考多方資訊、醫療器材實務、標準、指引,提供製造商從設計特性中,規格化醫療器材的生命期,達到歐盟醫療器材條例(MDR)要求。
此文逐次探討生命期的相關面向,由辭彙及定義、法規及標準要求、風險管理考量事項、醫療器材分級、設計及開發考量事項、文件化、做出生命期聲明等,呈現醫療器材生命期的現今情況。
按語1:此文引述歐盟醫療器材條例(EU MDR 2017/745)及相關指引文件,見引用之各項參考資料,俾益查閱文件原始出處及內容。
按語2:此文引述若干產業界實務從業者經驗報告,見引用之超連結內容,俾供點選查閱原始出處及內容。。
按語3:醫療器材生命期的規劃、評估、評鑑、試驗及撰寫聲明,宜配合各國醫療器材的相關法規,實務上靈活調整運用。
© All Rights reserved. 版權聲明。
生命期及名詞定義
貨架儲存期/貨架壽命 Shelf Life
指器材從成品的完成製造日期開始,若滅菌器材係指器材在初級包裝內完成滅菌程序起,且器材保持在原本初級包裝內,直到首次使用器材的期間,維持安全及有效,已知可以安全使用的時間期限。通常適用於具有某些特性的器材,該特性可能因為從製造出最終成品(或做成初級包裝、或完成滅菌程序)到首次使用期間逐漸衰減或耗散,原因可能是器材本身性質(例如:產品包含液體成分)、或包裝材料(例如:滅菌初級包裝袋)、或是器材中的某個組件(例如:電池)或成份(例如:化學品、液體)。貨架儲存期一般由製造商經由實際放置期間或模擬測試而決定之,例如:加速老化或實際使用時間測試,模擬運輸、儲存和使用前預處理的設想環境狀況等限制性條件。決定貨架儲存期因素,包括:用於製造器材的材料(包括:零件或材料是否逾期)、包裝材料、運輸/儲存條件等。貨架儲存期的終點是產品失效日期。超過此期限後,醫療器材將不再具有預期的性能參數及使用功能。有效期限 Expiration Date
指器材失去穩定性且不再按預期使用目的運作的日期,有效期屆滿之後,器材不再能安全使用,故不宜使用或須停止使用。通常「有效期」亦稱為「有效日期effective date」、「有效期限 effective duration」。從應用面考量,有效期限針對具有某些特性的產品,該特性會在一定時間範圍內衰減、耗散或降解,不限於該器材已經開始使用與否,例如:隱形眼鏡溶液中的酸度水準。
預期壽命 Expected Lifetime和生命期/使用壽命Useful Life
總括地說,此處的幾個名詞在實務上代表相同的意義,係指器材在製造出最終成品(或是完成初級包裝、或完成滅菌程序)、維持安全性及有效果,可以安全地滿足預期使用目的所達到的時間期限,通常為首次使用器材至以下3種情況之間的期間:- 已經使用在其預期目的之應用程序(例:一次性消耗品);
- 器材逐漸衰竭乃至逾期(例:產品包含液體成分),或是初級包裝拆封的瞬間(例:滅菌器材的初級包裝);
- 失效狀況漸漸轉變到未能接受的程度,或器材出現未能修復的故障(例:電子電氣或機械式醫療器材)。
生命(週期)結束 End of Life (cycle)
通常的解釋係指某種器材不再製造、提供售後服務及維護的時間,可能包括階段如下:- 器材已經停產、
- 製造商停止對器材的積極推廣(銷售壽命停止),儘管該器材可能仍然在銷售通路中被經銷商逐級地販售和/或提供維修支援;
- 終止對市場上仍在使用的器材提供維護和支援;
- 停止使用產品,意即將器材從醫療保健機構中移除或斷開、轉供替代使用(例:翻新、轉贈、汰舊換新)、除役或報廢。
服務壽命 Service Life
通常是製造商為仍在現場使用的器材提供服務及維護的期間,包括:網路安全(如果適用於該器材)。此時間範圍由製造商決定,除預期壽命和環境條件等因素外,製造商尚須考慮儲備物料或部件的成本和可獲得性等客觀因素。若是產品需要維修以延長使用期間,製造商須制定維修計畫,通知用戶器材即將停用、器材不再獲得原製造商提供服務及支援的時間。須預留充裕的前置時間,俾醫療保健機構考慮多種因應方案的優先程度及可行性,如:延長維修期、器材大修、更換器材、另購新器材。生命週期 Life Cycle
一般為貨架儲存期與生命期的組合,其中包括多個階段:器材生命週期可以從概念發想、設計、開發、製造,放入市場、首次使用、(若適用時)重複使用、直到器材報廢或除役而退出市場。例如:生命週期內,即使器材不再生產、或停止售後服務或維修,製造商仍應記錄被動地收集來的相關資料,將之納入後市場監督的一部分,如:收到對仍在現場產品的投訴和警戒資訊,並將此等資料盡可能地應用在更新風險管理、可用性工程評估、軟體績效檢討及臨床評估報告更版。歐盟醫療器材條例(EU MDR,2017/745)並未著墨在醫療器材生命期(lifetime)的定義,而在產品標準或法規指引中採用的定義,各抒意見,重點尚非一致,由此可能導致具有貨架儲存期的器材和可重複使用(reusable)的器材,出現某種不確定性情況。有鑒於此,器材生命期和貨架儲存期的定義係確保使用者和患者了解器材可企及的安全性和性能。使用者和患者需要知道器材的安全使用期間,從首次使用時間點開始,根據其預期目的評估該器材可以正常使用多久,仍然達到預期的安全性和性能。因此,製造商、使用者和患者之間清晰的溝通實屬必要,各方得以鑑別器材從首次使用到報廢或除役的生命期,亦須考慮此段期間維護器材所需要的各種活動。
參考上述,歐盟醫療器材條例亦未定義貨架儲存期。貨架儲存期對於受到有效期限約束的滅菌器材至關重要。但是,無論是否為滅菌器材,製造商務須考慮儲存情況作用在醫療器材本身,及可能衝擊醫療器材的安全性和性能。
生命期考量原則
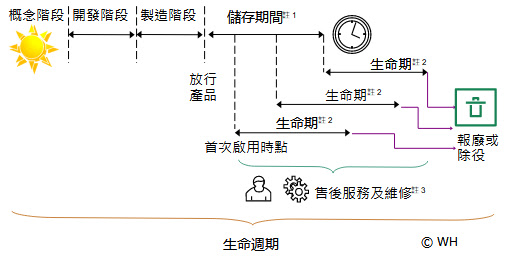
製造商不宜將貨架儲存期和生命期量測值,逕行結合而加總為概括的生命期數值,因為有許多種方式說明生命期;例如:每種程序的使用週期數,或清潔和滅菌的週期數。因此,在某些情況下,貨架儲存期加上生命期的代數和可能偏離現實,何不乾脆區分貨架儲存期和生命期,給出各自的數值。但是,在查證生命期時,製造商宜考慮貨架儲存期對生命期的衝擊,尤其當器材或其零部件與材料是否會隨著時間的推移而衰竭,以及在最惡劣情況下,以最長的貨架儲存期所儲存的器材,是否足以達到原本宣稱的生命期。製造商須考慮是否需要進行某些相關維護或更換器材或其零部件,以維持貨架儲存期。例如:電池可能會隨著時間的推移而失去儲存電量,或可能受到儲存條件的影響,而這程狀態又會影響零件和器材的生命期。生命期不宜與 ISO 14971 的生命週期(life cycle)相混淆,後者係包括器材設計和開發等各種階段。圖一展示的生命週期模型包括:器材的概念、開發、製造、首次使用、重複使用(若適用時,配合必要的維護及修整)、服務以及維護、報廢或除役。該模型慮及製造商支持業務管理,以及與所有活動的完整時間段:包括:設計、製造和上市後階段。而且,製造商得在每個產品生命週期階段影響和決定器材的生命期(參見圖一概略呈現上述原則)。
圖一描述貨架儲存期、生命期和生命週期,將生命期顯示為首次使用到報廢或除役的時間點。但是,對於具有既定的貨架儲存期器材,此處敘述的生命期得從貨架儲存期的任何一個時間點開始。製造商可由已規劃的預防性維護活動延長貨架儲存期和生命期,例如:在儲備電量耗盡之前須為電池充電、或者在預估可能發生故障前,更換已知會隨著時間的推移而磨損的零件、或貨架儲存期較短的零件,以避免該器材逾越貨架儲存期。
圖1:器材的生命期
註1:「儲存期間」係從製造日期到宣稱的使用截止日期(use-by date)的期間。並非所有器材都有使用截止日期。尚須考慮器材的儲存狀況、環境條件和經歷時間。
註2:後續使用器材的次數和/或期間。註3:採用售後服務和維修得以延長器材生命期。
註4:歐盟產品要求通告OJ EU 2022/C 247/01,亦稱「藍色指引」,第2.6節,單一產品的第一次開始使用日期各自計算,而非以單一批次的產品第一次開始使用的日期計算。
註5:圖1引用ISO 14971生命週期,係考慮醫療器材生命週期的所有階段,從最初的概念到最終的除役和報廢。
(未完,見續篇)
沒有留言:
張貼留言